
中大新聞網(wǎng)訊(通訊員熊嘯林)免疫源性細(xì)胞死亡(immunogenic cell death, ICD)是指腫瘤細(xì)胞在外界刺激的作用下介導(dǎo)機(jī)體產(chǎn)生抗腫瘤免疫響應(yīng)的過程,最早由Guido Kroemer課題組在研究蒽環(huán)類化療藥物多柔比星處理的細(xì)胞中發(fā)現(xiàn)。目前,已有包括米托蒽醌、奧沙利鉑等臨床使用的化療藥物被發(fā)現(xiàn)具有ICD活性。由于兼具抗腫瘤細(xì)胞毒性與激活抗癌免疫的能力,ICD藥物展現(xiàn)出了更好臨床應(yīng)用前景。然而,ICD藥物開發(fā)仍然面臨以下幾個阻礙:(1)具有ICD活性的抗癌小分子仍然較少;(2)當(dāng)前對于ICD現(xiàn)象的分子機(jī)理尚不明確。
近日,中山大學(xué)藥學(xué)院鄒滔滔教授課題組與廣西師范大學(xué)梁宏教授課題組合作,根據(jù)ICD與內(nèi)質(zhì)網(wǎng)應(yīng)激的較強(qiáng)聯(lián)系,發(fā)掘了出一個基于三價銥的抗癌金屬配合物(1a)具有良好的ICD活性。隨后,對該化合物的雙氮雜環(huán)卡賓配體進(jìn)行修飾,引入了光親和標(biāo)簽與疊氮基團(tuán),得到了可用于化學(xué)蛋白質(zhì)組學(xué)研究的探針分子。課題組進(jìn)而利用該探針抓取了一系列蛋白質(zhì)靶標(biāo)。
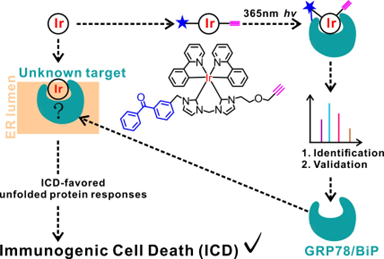
圖1. 化學(xué)蛋白質(zhì)組學(xué)揭示金屬銥配合物的靶蛋白BiP
基于其它ICD相關(guān)研究的線索,團(tuán)隊成員鎖定了ER stress的核心調(diào)控蛋白GRP78/BiP作為研究對象,通過一系列實驗驗證了1a可以通過降低BiP蛋白的穩(wěn)定性進(jìn)而抑制其活性。更有趣的是,已知的ICD藥物如米托蒽醌、奧沙利鉑等均可作用于BiP,預(yù)示了抑制該蛋白在激活I(lǐng)CD中的重要作用。最后經(jīng)過生物信息學(xué)分析發(fā)現(xiàn)BiP在三分之一以上的腫瘤類型中高表達(dá),具有抗腫瘤靶點(diǎn)潛力。綜上,本研究發(fā)展了一個新的ICD分子并基于化學(xué)蛋白質(zhì)組學(xué)等技術(shù)發(fā)現(xiàn)了BiP蛋白在ICD中的作用。
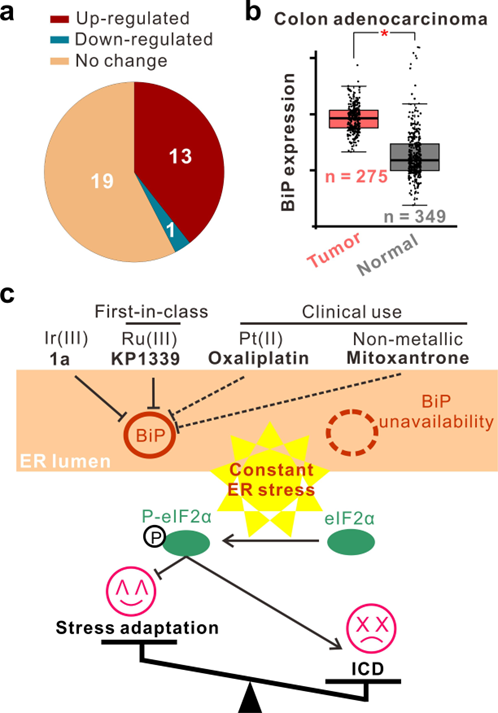
圖2. 多種ICD激活分子可以抑制BiP活性
該研究成果近日以Article形式發(fā)表在J. Am. Chem. Soc.上,中山大學(xué)為第一單位;中山大學(xué)藥學(xué)院博士后熊嘯林、廣西師范大學(xué)副教授黃克斌以及中山大學(xué)藥學(xué)院2019級專業(yè)碩士王園為論文的共同第一作者;中山大學(xué)藥學(xué)院鄒滔滔教授與廣西師范大學(xué)梁宏教授為共同通訊作者。該工作得到國家自然科學(xué)基金優(yōu)秀青年基金項目、國家自然科學(xué)基金青年科學(xué)基金項目、中國博士后面上項目、廣東省手性分子與藥物發(fā)現(xiàn)重點(diǎn)實驗室、廣東省珠江人才計劃青年拔尖人才、廣東省自然科學(xué)基金、廣州市科技計劃等項目支持。
論文鏈接:https://pubs.acs.org/doi/10.1021/jacs.2c02435