
中大新聞網訊(通訊員康新梅)近日,中山大學附屬第三醫院張琪、許燕團隊在Nature Communications在線發表了題為“Mettl3-mediated mRNA m6A modification controls postnatal liver development by modulating the transcription factor Hnf4a”的最新研究成果,系統闡述了Mettl3介導的m6A修飾在小鼠出生后肝臟發育成熟中的階段特異性作用。研究發現,Mettl3介導的m6A修飾是出生后肝臟發育過程必需的,但成年后敲除Mettl3不影響肝臟穩態維持。機制研究發現Mettl3缺失可導致Hnf4a等肝臟核心轉錄因子轉錄本上m6A修飾減少,降低Hnf4a mRNA穩定性,最終導致出生后早期小鼠肝臟發育受阻。
肝臟是機體最大的實質器官,也是新陳代謝的中心站。肝臟發育和成熟是一個復雜精細有序的過程,受到胞內外信號、表觀遺傳調控和轉錄調控等多層次嚴密調控。N6-甲基腺苷(m6A)是真核生物mRNA最豐富的修飾,調控轉錄、核質運輸、穩定性和翻譯等多個RNA代謝過程。m6A受到甲基化酶和去甲基化酶的動態調控,其中由催化亞基Mettl3和調節亞基Mettl14、 Wtap等組成甲基轉移酶復合物負責將m6A加載到轉錄本上特定位點,去甲基化酶ALKBH5或FTO負責移除m6A修飾。既往研究報道了m6A修飾參與干細胞分化、腫瘤發生等眾多生理病理過程。然而,m6A修飾在哺乳動物肝臟發育中的作用尚無系統研究。
研究發現,人和小鼠肝臟中m6A修飾水平以及甲基化酶復合物組分Mettl3和Mettl14表達水平在出生后肝臟發育不同階段動態變化,提示m6A修飾在哺乳動物出生后肝臟發育過程中發揮重要作用。出生前后肝細胞特異性敲除Mettl3(Mettl3flox/flox/Albumin-Cre,Mettl3 cKO)的小鼠出現明顯的肝臟脂質沉積、肝細胞凋亡、肝纖維化以及肝前體細胞活化等肝損傷表現,最終在出生后4-7周死亡,說明Mettl3在出生后小鼠肝臟發育中有著不可或缺的作用。
通過m6A-RIP-sequencing和RNA sequencing和一系列驗證分析,研究人員發現肝臟中包括Hnf4a在內的一系列肝臟核心轉錄因子的mRNA上存在m6A修飾。敲除Mettl3后,這些基因轉錄本上的m6A修飾明顯減少,導致Hnf4a的mRNA和蛋白水平及其下游靶標的表達量顯著下調。應用腺相關病毒在肝細胞中特異性過表達Hnf4a可以部分緩解Mettl3 cKO小鼠肝損傷,延長存活時間。機制研究發現,敲除Mettl3導致肝細胞中Hnf4a mRNA穩定性下降,這一作用依賴于m6A閱讀蛋白Igf2bp1。這些數據說明Mettl3介導的m6A修飾以Igf2bp1依賴的方式促進肝臟核心轉錄因子Hnf4a mRNA穩定性,維持小鼠出生后肝臟發育。
研究人員進一步探究了Mettl3及其介導的m6A修飾在成體小鼠肝臟穩態維持中的作用。通過構建肝細胞特異性可誘導敲除Mettl3的小鼠(Mettl3flox/flox/Alb-CreERT2,Mettl3 icKO),研究者發現成年后敲除Mettl3不影響小鼠肝臟穩態維持。
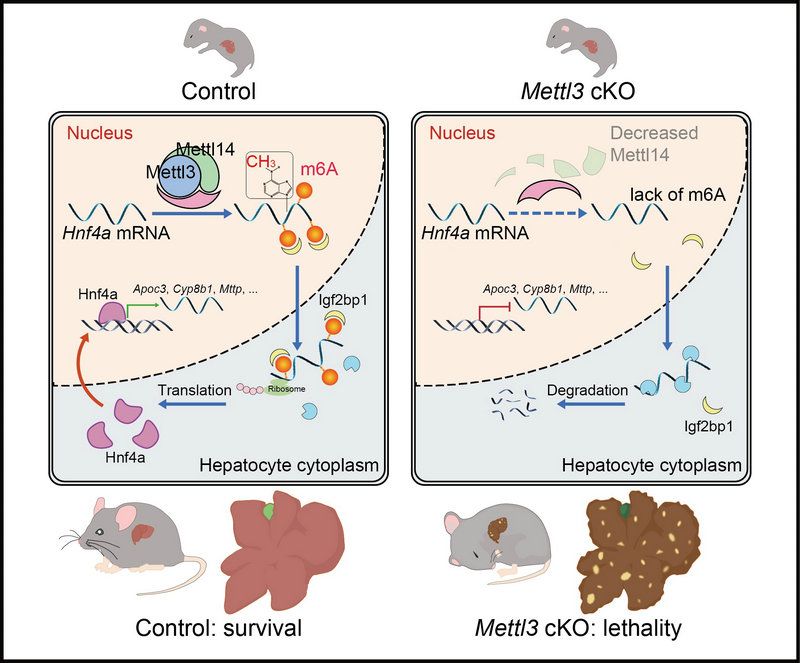
機制圖
本研究系統闡述了Mettl3介導的m6A修飾在小鼠出生后肝臟發育成熟中的階段特異性作用,發現Mettl3介導的m6A修飾是出生后肝臟發育早期必需的,但成年后敲除Mettl3不影響肝臟穩態維持。本研究揭示了肝臟發育成熟的表觀遺傳調控新機制,為肝臟發育相關重大疾病防治提供了新思路。
張琪、許燕研究團隊長期專注于肝臟疾病發生發展的表觀遺傳調控機制研究及肝臟疾病的細胞治療研究。在Cell Stem Cell, Journal of Hepatology, Nature Communications, Molecular Therapy等雜志發表多篇文章,先后獲得國家重點研發計劃、國家自然科學基金面上項目等多個基金支持。
該論文第一作者為中山大學附屬第三醫院許燕副研究員、科研助理周卓偉(現為密歇根大學博士研究生)和博士研究生康新梅,通訊作者為張琪教授。